免费热线
400-996-3155

简介:
高效无缝克隆试剂盒是一种混合酶系统,包含了DNA 5' 外切酶(5' Exonuclease)、DNA聚合酶(DNA Polymerase)和DNA连接酶(DNA Ligase)活性的重组酶。利用特殊的重组酶和同源重组原理,其可将任意方法线性化的载体和与其两端具有15-25bp重叠区域的PCR 片段定向重组连接,可以实现1-7个片段的高效无缝拼接。
该试剂盒通过精心设计和严格试验,使用非常简单,不依赖于 T4 DNA 连接酶,不受载体和目的片段的酶切位点限制,只需加入合适比例的载体和 PCR 片段在室温孵育15-30 min 即可完成 PCR 片段高效定向无缝克隆至载体的任意位置,从而获得完整的双链 DNA 分子。
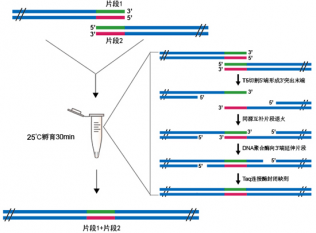
5' 外切酶可从双链 DNA 5'端切割形成 3'突出末端, 从而促进重叠区域的具有互补序列的片段进行退火。高保真 DNA 聚合酶可使退火的片段向 3'端延伸,从而填补片段缺口。Taq DNA 连接酶可封闭缺刻,最终得到的无缺口闭环质粒可直接转化感受态细胞筛选克隆,3-4小时内即可完成从DNA样品的PCR扩增、纯化、重组、到转化涂板的全部操作。其中PCR反应约2-3小时,PCR产物纯化约20分钟,重组反应15分钟,转化涂板约40分钟,共计3-4小时即可完成。
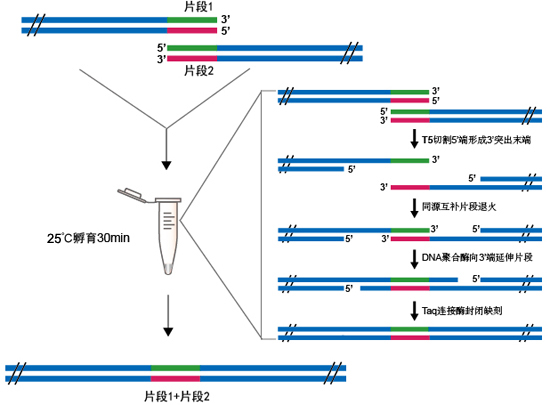
Fig.1 高效无缝克隆原理示意图
1. 快速:室温孵育15分钟即可完成片段的连接。
2. 方便:不受载体或插入片段酶切位点限制在任意位置进行无缝克隆
3. 简单:不依赖于 T4 连接酶,高效连接,无碱基缺失。 插入片段的PCR产物正确且单一,无需纯化,可直接与载体进行重组反应。
4. 无缝:可同时高效连接一个或多个 PCR 片段,不引入额外序列。
5. 高效:无需额外的亚克隆,菌检阳性率高达 95%。
6. 范围宽:从20bp左右的小片段到10kb左右的大片段都可以成功插入
7. 特异性:只有插入片段和线性化载体的末端才能发生同源重组,可以有效避免非特异性的同源重组;
1. PCR/酶切制备线性载体
(1)酶切获得:单酶切或双酶切均可获得线性化载体,选用的内切酶不同,载体会产生粘末端和平末端;酶切后的载体进行胶回收后再用于高效无缝克隆,这样有助于减少转化时因酶切不完全导致的假阳性克隆。建议使用双酶切,载体线性化完全,转化背景低。
(2)PCR 扩增获得:建议用SupersmartTM Z5 超保真 DNA聚合酶(货号:ZS-M12005)进行 PCR 扩增载体片段, 获得的产物建议用凝胶回收纯化以降低转化后的假阳性克隆。在以载体为模板进行 PCR 扩增时,模板的量应控制在 0.1-0.5 ng/50 μl 体系,从而降低转化背景。一般而言,凝胶回收后,非线性化载体已降低至一定程度,可以直接应用于高效无缝克隆。
*建议通过 PCR 扩增获得线性化载体,这样可最大程度的降低转化背景(空载体),提高连接效率和转化阳性率。
2. 用包含重叠序列的引物扩增片段
应用SupersmartTM Z5 超保真 DNA聚合酶(货号:ZS-M12005)进行 PCR 扩增获得插入片段,获得的片段如产物单一条带可进行 PCR 产物纯化回收,否则进行凝胶回收以提高转化效率和克隆阳性率。插入片段的引物设计尤其值得注意,插入片段的引物序列包括重叠序列部分和特异性部分。通过在引物 5’端引入线性化克隆载体末端的同源序列,使得插入片段的 5'和 3'端分别带有与线性化克隆载体两端对应的完全一致的序列,重叠区域的长度一般为 15-25 nt,对于长片段可增加至 40nt 同源序列,特异性部分在 18-25 nt。
2.1 单个插入片段的引物设计
(1)酶切获得线性化载体
根据载体线性话方式不同,其末端结构包括 5'突出末端、3'突出末端和平末端三种形式,引物设计也分三种情况。线性化载体上的重叠序列只能用酶切后的3' 端序列进行计算。特别是对于酶切后产生5' 端突出的情况,不能以5' 端突出部分计算重叠序列,因为重组反应时有DNA 5' 外切酶(5' Exonuclease)活性,会消化掉5' 端序列。示意如下:
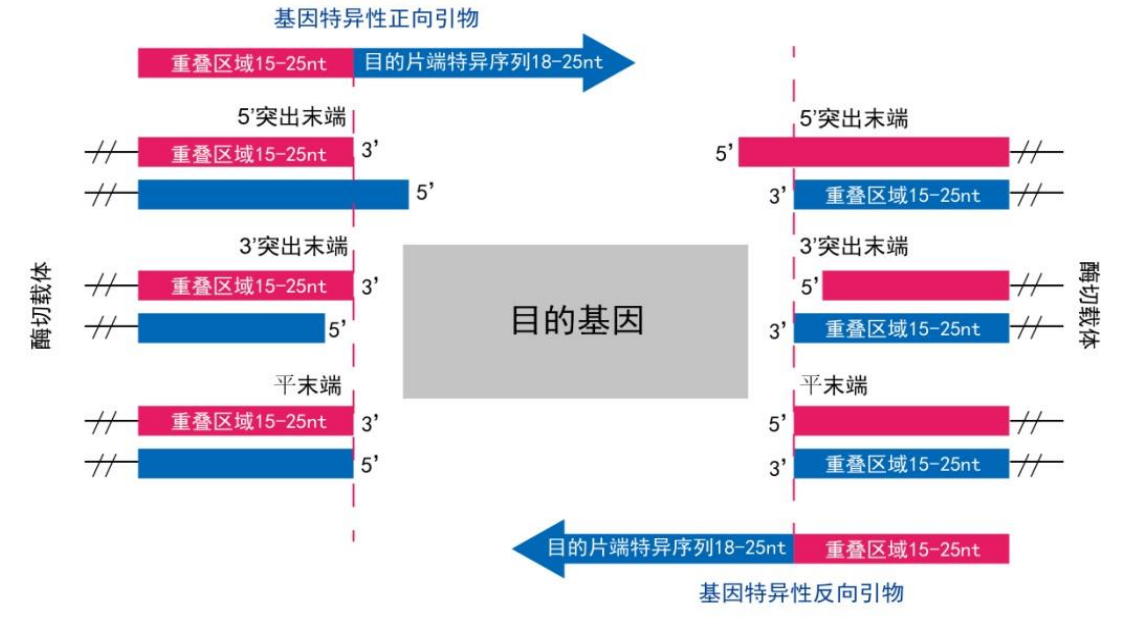
Fig.2 酶切获得线性化载体与插入片段连接引物设计示意图
(2)PCR 扩增获得线性化载体
线性化载体由反向 PCR 扩增获得时,要求扩增载体的 PCR 引物和扩增插入片段的对应 PCR 引物的重复序列在15-25 nt 之间。如只需连接一个基因,可将重复序列分配在载体和插入片段上(Fig3),这样引物易于优化;如需连接多个基因,为减少载体扩增次数,可将重复序列只设计在载体上(Fig4)。
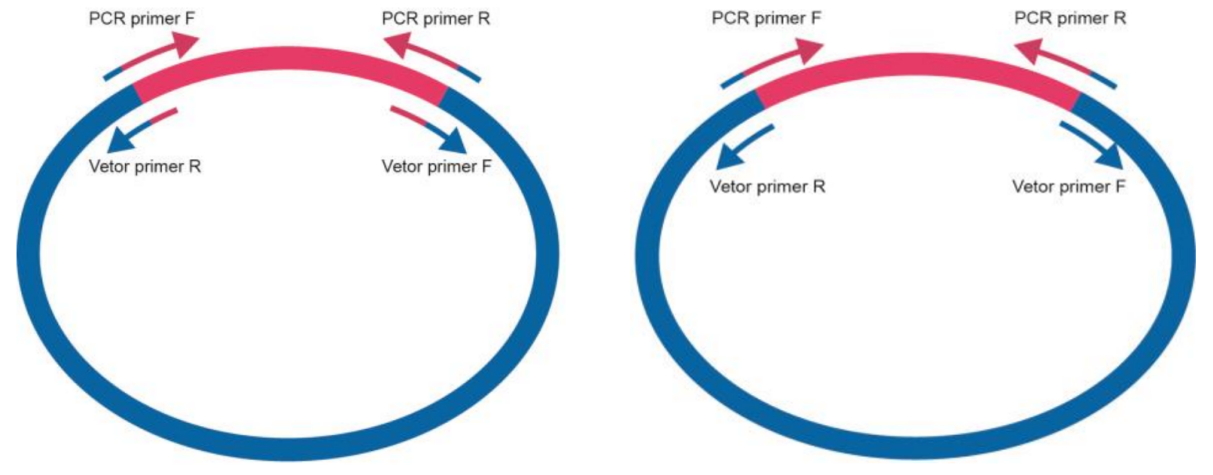
Fig3 Fig4
2.2 多个插入片段的引物设计
多个插入片段引物设计原理同单片段,即相邻片段之间有 15-25 nt 的重叠区域, 设计引物时有两种方式(Fig5),一种为重叠区域分配在两个片段,另一种为重叠区域完全在其中一个片段上。重叠序列宜尽量设计为8个G或C和8个A或T,同时使退火温度不低于48℃(以AT配对为2℃,GC配对为4℃进行粗略计算)。设计如下图例:
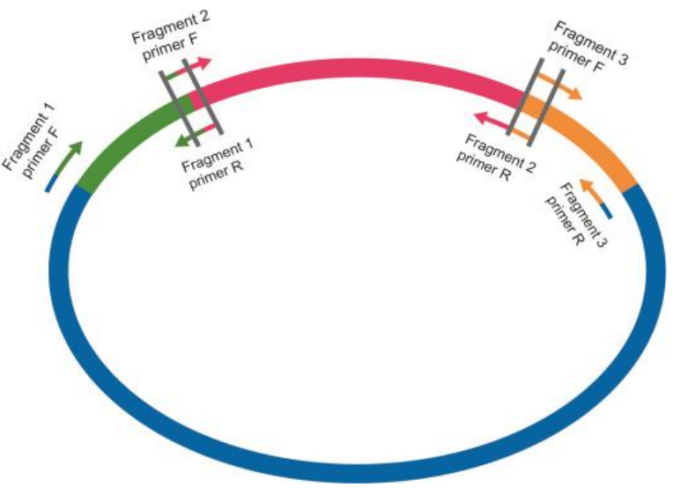
Fig5
3. 载体片段和 2×Effcienct Seamless Clone Mix混匀重组
3.1 取出 2×Effcienct Seamless Clone Mix,放置于室温使其完全溶化或用手捂化,融化后轻弹混匀,再短暂离心,以免有贴在管壁或管盖上的造成损失。
3.2 准备好线性化载体和插入片段,按照下表配制反应体系
线性化载体 | 10-50 ng |
插入片段 | x* μl |
2×Effcienct Seamless Clone Mix | 5 μl |
灭菌水 | up to 10 μl |
注:线性化载体一般 10-50ng/10μl 反应体系,插入片段与载体的摩尔比为 4-5:1 最佳。
DNA 片段的摩尔数算法如下:
pmols = (质量 ng) x 1000 / (碱基数量 x 650)
50 ng of 5000 bp 双链 DNA 片段相当于 0.015 pmol
50 ng of 500 bp 双链 DNA 片段相当于 0.15 pmol
3.3 轻轻混匀,于 PCR 仪上 25℃孵育 30min,反应产物用于转化或冻存于-20℃。对于短片段(<1kb)或 1-2 个片段,孵育时间可缩短至 15min,对于较长片段或多片段连接,可延长孵育时间至 60min,适当延长孵育时间可提高连接效果。
4. 转化
4.1 取5-10μl上一步骤的反应样品加入到50-100μl DH5α等感受态细胞中(注意所加入的DNA样品体积不要超过感受态体积的1/10),轻轻混匀,将该混合物置于冰上30min。
4.2 42℃水浴中90秒进行热激,然后迅速放回冰浴中,静置3~5min。
4.3 加入500 μl不含抗生素的SOC或LB培养液,轻轻混匀,37℃震荡培养1h。
4.4 将菌液5000 rpm离心1 min以沉淀菌体。吸去大部分培养液,剩余约50-100μl的培养液,重悬菌体。然后全部均匀涂布到含适当抗生素的LB平板上,37℃培养箱中培养过夜。
4.5 第二天挑取平板上的克隆进行菌落PCR或者提取质粒进行酶切鉴定,也可以挑取至少 3 个克隆进行测序验证。
常见问题:
1、无克隆长出或克隆数较少
可能原因如下:
(1)引物设计不理想:根据 15-25nt 同源序列+18-25nt 基因特异性引物原则设计优化引物,引物 GC 含量在 40—60%之间,Tm 值>50℃。
(2)感受态细胞的效价过低:使用的感受态细胞效价要>106 cfu/μg,操作时可设置转化质粒的实验对照,以排除因感受态细胞的效价过低引起的失败。
(3)线性化克隆载体与插入片段的使用量过少或比例不佳:按照上述操作步骤中建议的量配制反应体系,载体一般使用量为 10-50 ng,插入片段与载体的摩尔比为 4-5:1 最佳,如比例严重不合适会降低转化效率。
(4)线性化载体或插入片段未进行纯化抑制连接反应:线性化载体无论是酶切获得还是 PCR 扩增获得,都建议进行凝胶回收后再用于高效无缝克隆,插入片段 PCR 扩增后,如未经纯化,体积不要超过总反应体积的 20%。
(5)感受态细胞对重组反应体系过敏。使用水对重组后的反应液稀释5-10倍后再进行转化。
(6)转化细菌时重组反应样品加入过多。确保重组反应样品的体积不超过感受态细胞体积的10%。
(7)选择了错误的抗生素,或在固体LB培养基中加入了过量抗生素。涂板时选择正确的抗生素和浓度。
2、 出现较多假阳性(空载体)
(1)克隆载体酶切不完全或 PCR 扩增时加入模板过量:未完全切开的载体会导致转化背景,即假阳性克隆,可通过提高限制性内切酶使用量、延长酶切反应时间、胶回收纯化酶切产物来降低未切开载体导致的假阳性。
(2)PCR 扩增克隆载体时,每 50 μl 体系模板的量控制在 0.1-5 ng,否则也会导致转化背景过多。
3、克隆测序后片段不正确
(1)PCR 产物混有非特异扩增产物:建议优化PCR反应引物设计以增加PCR产物的特异性,并对 PCR 产物进行切胶回收,保证回收的条带为正确的单一条带。
(2)酶切不完全:如线性化载体时不是由空载体酶切或扩增,而是由已插入其他片段的载体酶切或扩增制备而来,酶切不完全会导致克隆中插入不正确的片段,因此提高酶切效率或使用预线性化质粒作为模板或载体凝胶回收都可降低此种情况的发生。
储存:
-20℃可保存 2 年,-80℃可保存 5 年,避免反复冻融。
相关产品:
货号 | 产品名称 |
ZS-M11001 | |
ZS-M11002 | |
ZS-M11003 | |
ZS-M11004 | |
ZS-M11006 | |
ZS-M11011 | |
ZS-M11012 | |
ZS-M12002 | |
ZS-M12003 | |
ZS-M12004 | |
ZS-M12005 | |
ZS-M12006 | |
ZS-M12007 | |
ZS-M12008 | |
ZS-M12009 | |
ZS-M12010 | |
ZS-M12011 | |
ZS-M12012 | |
ZS-M16001 | |
ZS-M16004 | |
ZS-M18001 | |
ZS-M18002 | |
ZS-M18004 | |
ZS-M18005 | SupersmartTM DNA气溶胶污染消除剂 |
ZS-M18006 | |
ZS-M18011 |

 400-996-3155
400-996-3155